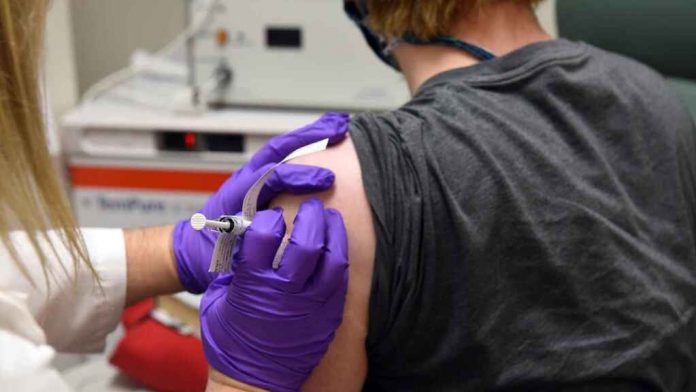
Mientras que este fin de semana la vacuna contra el coronavirus de Oxford ha retomado sus ensayos clínicos tras el parón por enfermedad de un voluntario, hoy han arrancado las primeras pruebas con humanos en España.
La farmacéutica Janssen, empresa de Johnson&Johnson, probará las dosis en 190 españoles. Aunque las pruebas iban a empezar hoy en los hospitales La Paz y La Princesa de Madrid, finalmente se inician en Santander. Según la Agencia EFE, el aplazamiento se debe a un «problema» con el laboratorio.
Por tanto, serán los 40 voluntarios del Hospital Marqués de Valdecilla los primeros en recibir la dosis de la vacuna. El martes será el turno de los hospitales madrileños en los que participan otros 150 voluntarios, 75 de cada centro. No obstante, España no es el único país participante del estudio. Para el ensayo de la segunda fase se han incluido un total de 550 voluntarios sanos de diferentes países.
Todos ellos son personas de entre 18 a 65 años que han demostrado estar sanos y sin haber padecido el coronavirus. Además, ningún voluntario ha estado en contacto con positivos y se ha garantizado que tienen riesgo bajo de contagio.
UNA FASE DE HASTA SEIS MESES DE ESTUDIO
Esta nueva fase de estudio durará previsiblemente entre cuatro y seis meses. Tras recibir la primera dosis, se realizará un seguimiento semanal de los voluntarios durante un mes. Entonces recibirán una segunda dosis y volverán a someterse a seguimiento clínico semanalmente. Al final contarán con una media de 12 a 14 visitas repartidas entre los dos y cuatro meses de ensayo.
Respecto a la existencia de riesgos, la respuesta de los expertos es que los voluntarios no están libres de peligro. El investigador principal y coordinador de la Unidad de Ensayos Clínicos del Hospital La Paz, Alberto Borobia, afirmó que «ningún tratamiento es inocuo». No obstante, aseguró que la agencia reguladora no aprueba ensayos clínicos si no hay datos que garanticen la posibilidad de su administración a personas voluntarias.